来源:广西肝脏疾病免疫与代谢研究重点实验室 发布时间:2026-03-06 作者:姚美 校对:韦载娲 审核:钟伏弟 浏览量:次
![]()

饮酒与 HBV 感染的协同作用是驱动肝癌发生发展的重要诱因,但其背后的核心分子机制仍有待阐明。LPLA2作为溶酶体内关键的代谢调控酶,参与溶酶体磷脂代谢的精细调控;而双单酰甘油磷酸(bis(monoacylglycero)phosphate, BMP)作为溶酶体特异性磷脂,其代谢异常与肿瘤代谢重编程密切相关。本研究聚焦于酒精与 HBV 协同促癌的分子通路,旨在明确 LPLA2 及BMP代谢在这一过程中的关键作用及调控机制,为肝癌的精准防治提供新的理论依据。
关键发现
1.酒精显著加速HBV相关HCC发生发展:利用HBx转基因小鼠和裸鼠异种移植模型发现,长期酒精摄入可显著促进小鼠自发性HCC形成,加速皮下肿瘤生长,增加肿瘤数量与体积,并提升肝癌标志物AFP的表达水平。进一步的机制研究显示,酒精代谢产物乙醛是介导这一促癌效应的核心介质。
2.酒精诱导HBV相关HCC中BMP磷脂特异性蓄积:脂质组学分析显示,乙醇喂养的HBx转基因小鼠肿瘤组织中,BMP是富集最为显著的脂质类别,10种BMP亚型水平均大幅升高。深入分析发现,BMP的异常蓄积依赖于LPLA2的上调:酒精可提升HCC细胞中LPLA2的表达和酶活性,而敲低LPLA2则可抑制乙醇诱导的BMP蓄积,提示LPLA2是酒精调控BMP代谢的核心节点。
3.酒精通过ER应激/ATF4通路转录激活LPLA2:那么,酒精如何上调LPLA2?研究表明,慢性饮酒可诱导HCC细胞发生内质网应激,进而激活转录因子ATF4;激活后的ATF4可直接结合LPLA2编码基因启动子的关键区域,通过转录激活上调LPLA2表达。功能实验进一步证实,抑制内质网应激可完全阻断乙醇诱导的LPLA2上调,从而确立了ATF4作为调控LPLA2的核心分子地位。
4.VPS13C介导ER-溶酶体脂质转运为BMP合成提供底物:LPLA2的上调仅是BMP合成的一个环节,其合成过程还需充足的底物供给。由于BMP的合成以磷脂酰甘油(Phosphatidylglycerol, PG)为前体,而溶酶体本身缺乏PG,研究进一步发现,酒精诱导的内质网应激可增强ER-溶酶体接触,并借助脂质转运蛋白VPS13C将ER中的PG转运至溶酶体,从而为LPLA2催化合成BMP提供必要的底物来源。这一发现完善了BMP合成的完整链条。
5.LPLA2/BMP通过激活MAPK/ERK通路促进HCC细胞增殖:BMP蓄积之后如何驱动HCC进展?功能实验显示,LPLA2过表达在体内外均可显著促进HCC细胞增殖、加速细胞周期G1/S转换,而敲低LPLA2则抑制肿瘤生长并促进癌细胞凋亡。机制上,LPLA2催化产生的BMP可特异性激活MAPK/ERK信号通路,进而上调c-MYC、Cyclin D1等增殖相关分子的表达;更重要的是,使用ERK抑制剂或中和BMP均可完全逆转LPLA2的促癌效应,证实BMP-MAPK/ERK是该通路的核心下游机制。
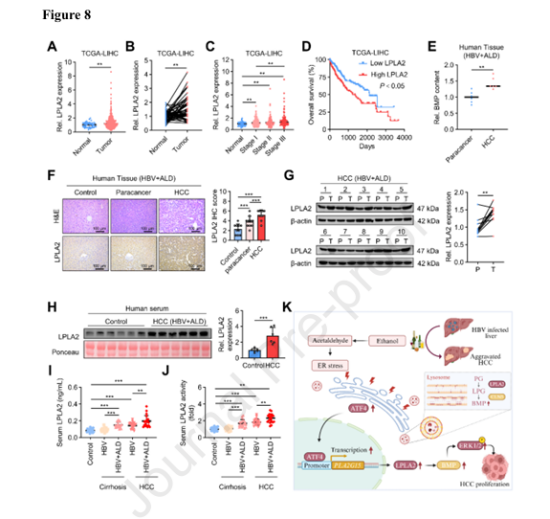
6.LPLA2在HCC中高表达且与不良预后密切相关:结果显示,LPLA2在HCC组织中的表达显著高于癌旁组织,且在HBV合并酒精性肝病的HCC患者中,其组织表达水平和血清酶活性均为最高;生存分析表明,LPLA2高表达与HCC病理分期进展相关,是HCC患者总生存期缩短的独立危险因素。
创新与意义
本研究首次阐明了“酒精-乙醛-内质网应激-ATF4-LPLA2-BMP-MAPK/ERK”这一信号轴,揭示了酒精通过调控溶酶体磷脂代谢增强HBV相关HCC发生发展的核心机制,填补了该领域空白。研究证实LPLA2是HBV合并酒精性肝病相关HCC的关键促癌分子,靶向抑制LPLA2或阻断BMP代谢可有效抑制酒精助推的HCC进展,为精准治疗提供了新靶点;同时,LPLA2的组织表达水平和血清酶活性可作为HCC不良预后的潜在标志物。
所有版权@广西肝脏疾病免疫与代谢研究重点实验室 ICP备案号: 桂ICP备05004851号-3
所有版权@广西肝脏疾病免疫与代谢研究重点实验室 ICP备案号: 桂ICP备05004851号-3