来源:广西肝脏疾病免疫与代谢研究重点实验室 发布时间:2025-07-07 作者:姚美 校对:韦载娲 审核:钟伏弟 浏览量:次
![]()
展现巨大潜力
2025年6月,《Nature》杂志在线发表了一篇题为《Targeting PIKfyve-driven lipid metabolism in pancreatic cancer》的论文,详细描述了PIKfyve在胰腺导管腺癌(PDAC)中的作用机制以及靶向PIKfyve和KRAS-MAPK信号通路的联合治疗策略,为PDAC的治疗提供了新的希望。

【原文链接】:Targeting PIKfyve-driven lipid metabolism in pancreatic cancer - PubMed
研究背景
PDAC作为预后极差的癌症之一,其五年生存率仅为13%。其肿瘤微环境以间质纤维细胞和细胞外基质沉积为特征,导致肿瘤细胞面临营养获取困难。为了适应这种营养匮乏的环境,PDAC细胞发展出了高效的自噬和溶酶体依赖途径,以获取生物合成中间体、调节铁稳态、降解MHC-1以逃避免疫监视等。这些途径在PDAC的代谢中起着重要作用,因此,靶向这些途径被认为是治疗PDAC的潜在策略。
关键结果和结论
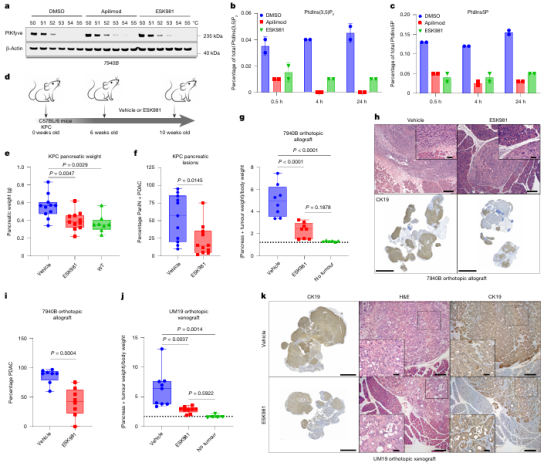
PIKfyve在PDAC中的作用:PIKfyve的缺失显著延长了携带KC(Ptf1a-Cre; LSL-KrasG12D/+)基因型小鼠的生存期,并减少了胰腺重量和PDAC病变。PIKfyve抑制剂能显著减少PtdIns(3,5)P2和PtdIns5P28的水平,并有效抑制PDAC的发展和生长。
PIKfyve抑制的代谢影响:PIKfyve抑制导致PDAC细胞上调脂肪合成的转录和代谢程序,特别是依赖于甾醇调节元件结合蛋白(SREBPs)的基因。另外,PIKfyve抑制导致PDAC细胞将更多的碳源从葡萄糖转移到脂肪合成中,尤其是鞘脂类。
联合治疗巨大潜力:联合应用PIKfyve抑制剂与KRAS-MAPK抑制剂(例如trametinib和selumetinib),在多种PDAC模型中显著降低了肿瘤负荷,且在部分模型中促使肿瘤完全消退。这一结果表明,联合治疗策略具有快速转化和临床应用的潜力。
研究创新
本研究借助遗传工程小鼠模型及药物抑制实验,精准锁定PIKfyve在PDAC进展中的关键角色,并创新性地提出靶向PIKfyve与KRAS-MAPK信号通路的联合治疗新思路。在此基础上,研究团队精心优化代谢分析流程,巧妙融合CRISPR筛选与RNA-seq技术,深度剖析PIKfyve抑制对PDAC细胞代谢的全方位影响。这一联合治疗方案在显著削减肿瘤负荷的同时,为PDAC治疗领域注入全新活力,开辟崭新研究方向。
研究意义
本研究深入阐释了PIKfyve在PDAC中的核心作用机制,前瞻性地提出靶向PIKfyve与KRAS-MAPK信号通路的创新治疗策略。鉴于KRAS-MAPK抑制剂及PIKfyve抑制剂在临床开发层面的积极进展,该联合治疗方案有望为PDAC患者带来突破性治疗选择,极大提升患者预后与生存率。后续研究将聚焦于进一步挖掘该联合治疗策略的临床应用潜力,全力推动PDAC治疗迈向新台阶。
所有版权@广西肝脏疾病免疫与代谢研究重点实验室 ICP备案号: 桂ICP备05004851号-3
所有版权@广西肝脏疾病免疫与代谢研究重点实验室 ICP备案号: 桂ICP备05004851号-3